Jūsų dėmesiui – pirmasis mokslo populiarinimo konkurso darbas. VU Fizikos fakulteto studentė Miglė Anušauskaitė pasakoja apie Boro (Bohr) atomo modelį, kodėl jis klaidingas, bet vis išlieka populiarus. Kalba netaisyta, skaitykite po kirpsniuku. O jei manote, kad galite geriau (arba tiesiog norite papasakoti apie savo mėgiamą sritį), nepabijokite sudalyvauti!
Atomas ir kiti gražūs rutuliai
arba
Kodėl neblėsta Bohro atomo modelio populiarumas?
Miglė Anušauskaitė
Rutulys, aplink kurį simetriškomis orbitomis skraido kiti, mažesni rutuliai – su tokiu atomu susipažinome mokykloje, tokį jį įsivaizduojame iki šiol. Ir tai nestebina: juk šiame modelyje naudojamos atomo savybės (neigiamo krūvio dalelės, jų išsidėstymas) eksperimentiniais duomenimis buvo patvirtintos jau prieš 100 metų.
Bet ar tai reiškia, kad per šimtmetį nesužinojome nieko naujo apie atomo sandarą? Anaiptol! Dabar jau žinome, kad dalelės, kurias laikėme nedalomomis, yra sudarytos iš kitų dalelių, o kai kurios šių dalelių savybės stulbina ir keisčiausioms teorijoms pasiruošusius mokslininkus. Fizikai, dirbantys su elementariosiomis dalelėmis, atomą mato visai kitaip, negu mes. Jei tokio fiziko draugijoje nupiešite atomą kaip vienas aplink kitą skriejančius rutuliukus, fizikas į jus pašnairuos kaip į žmogų, kuris ploja katučių nusileidus lėktuvui. Bet, užuot pykę ant šio fiziko, verčiau išsiaiškinkime, ką gi jis nuo mūsų slepia ir kodėl mums taip patinka tie vienas aplink kitą skriejantys rutuliai.
Atomo modelio vystymasis iki Bohro modelio
Įsivaizduokime, kad esame senovės Graikijoje ir su bičiuliais diskutuojame, iš ko sudarytas pasaulis. Vienas sako – iš vandens, kitas – iš skirtingos kondensacijos oro, trečias – iš ugnies, juk ji tokia dinamiška! O graikų filosofas Demokritas teigia, kad pasaulis sudarytas iš kietų, nuolatos judančių dalelių, tokių mažų, kad jų padalinti į dar mažesnes neįmanoma. Kadangi esame senovės Graikijoje, neturime pakankamai gerų priemonių patvirtinti arba paneigti šį teiginį, bet pripažinkime – idėja nebloga.
Daug vėliau – XIX amžiuje – chemikas Johnas Daltonas suformulavo tokias prielaidas: medžiaga sudaryta iš atomų, kurių negalima pagaminti ar sunaikinti. Visi tam tikros medžiagos atomai yra vienodi, o skirtingų medžiagų atomai skiriasi. Atomams pakeitus padėtį, įvyksta cheminės reakcijos. Šis chemikas atomą vaizdavo kaip rutulį – taisyklingą figūrą, kurios visi paviršiaus taškai vienodai nutolę nuo centro. Jo logiką sunku paneigti: bet kokia kita figūra verstų kelti klausimus apie jos nereguliarumus. Jei kubas – kodėl jo kampai atsikišę? Jei cilindras – kas jį verčia būti pailgu? Įsivaizduojant savipakankamą figūrą, „kabančią“ tuštumoje, rutulys šauna į galvą pirmiausia.
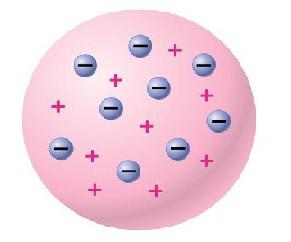
Didieji pokyčiai atomo teorijoje įvyko pirmajame XX amžiaus ketvirtyje. Dar 1897 m. britų fizikas J. J. Thomsonas eksperimentais įrodė, kad atome esama neigiamo krūvio dalelių – elektronų. Žinodamas, kad atomas neturi krūvio (t. y. yra neutralus), J. J. Thomsonas spėjo atome egzistuojant ir teigiamą krūvį. 1906 m. jis pasiūlė „slyvų pyrago“ modelį, kur rutulio formos atomas buvo įelektrintas teigiamai, o elektronai, kaip slyvos pyrage, išsibarstę teigiamo krūvio aplinkoje.
Tačiau Thomsono modelis neišsilaikė ilgai – jau 1911 m. Ernestas Rutherfordas pasiūlė naują atomo modelį. Atlikęs eksperimentus su α dalelėmis (helio branduoliais)E. Rutherfordasįsitikino, kad teigiamas krūvis yra susitelkęs mažoje atomo dalyje (branduolyje), o neigiamo krūvio elektronai skrieja aplink jį. 1913 m. Neilsas Bohras pasiūlė papildyti šį modelį elektronų orbitalėmis – mat jis įrodė, kad elektronai aplink branduolį yra išsidėstę „sluoksniais“. Peršokdami iš arčiau branduolio esančios orbitalės į toliau esančią elektronai suvartoja energiją, o peršokdami arčiau branduolio – atiduoda. Tai ir yra mums labiausiai pažįstamas atomo modelis, reprezentuojantis šią dalelę tiek logotipuose, tiek mokykliniuose vadovėliuose.
Kas vyko toliau?
Sekdami tolesnę atomo modelio istoriją nustebsime – praėjus vos 11 metų nuo populiariojo Bohro modelio išgryninimo, Louisas-Victoras de Broiglie’is pasiūlė jam alternatyvą! Tuo metu jau buvo žinoma, kad fotonai – šviesos kvantai – gali elgtis ir kaip dalelės, ir kaip bangos. De Broiglie’is pasiūlė hipotezę, kad ne tik fotonai, bet ir materiją sudarančios dalelės turi bangų savybių.
Taigi de Broiglie’is teigė, kad dalelė mums pasirodys kaip materija arba kaip banga priklausomai nuo to, kaip į ją žiūrėsime, tiksliau – kokį jos parametrą norėsime apskaičiuoti. Šitai buvo išradingai pritaikyta atomo modelyje – judėdami aplink branduolį elektronai elgiasi ne kaip maži skraidantys rutuliukai, o kaip aplink branduolį išsidėsčiusios bangos (bangą čia galime įsivaizduoti kaip vibruojančią gitaros stygą, kurios galai yra sujungti). Skirtingų orbitalių bangos nepersikloja ir išsilaiko savo vietoje, tarsi aplink branduolį būnančios orbitalės.
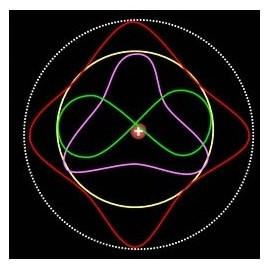
Bet neužtenka aprašyti, kaip reiškiniai vyksta tuomet, kai juos stebime – norint pagausinti žinias apie pasaulį, siekiama aprašyti, kaip reiškiniai vyksta tuomet, kai jų nestebime, surasti, koks slaptas mechanizmas glūdi už stebimų reiškinių savybių. Jei žinome, kad vien stebėjimu užfiksuotos reiškinių (tokių kaip atomai) savybės nėra pakankamos norint juos visiškai apibūdinti, galime imtis tikimybių. Būtent taip ir padarė Erwinas Schrödingeris, pasiūlęs tikimybinį atomo modelį. Tikimybių debesėlis aplink atomo branduolį nurodo, kokia tikimybė yra tam tikroje vietoje surasti elektroną, jei bus atlikti matavimai. Tai nereiškia, kad nustatydami elektrono padėtį tiesiog kažkurioje vietoje užfiksuojame itin greitai skraidančią dalelę. Tokios sistemos kaip atomai egzistuoja daugybėje būklių vienu metu (pavyzdžiui, elektronas vienu metu egzistuoja visose tikimybių debesėlio numatomose vietose) ir tik įsikišimas (toks kaip stebėjimas) priverčia superpoziciją kolapsuoti į vieną iš galimų būklių (pavyzdžiui, surasdami elektrono buvimo vietą priverčiame jį iš buvimo daugelyje vietų vienu metu kolapsuoti į buvimą vienoje vietoje).
Galime pastebėti, kad kiekvienas iš pateiktų atomo modelių koncentruojasi į konkretų atradimą atomo teorijoje: Thomsono modelis pateikia elektronų reprezentaciją, Bohro – orbitalių ir branduolį sudarančių dalelių, de Broiglio – banginės medžiagos prigimties ir t.t. Nė vienas iš modelių nepateikia visko, ką šiuo metu žinome apie atomą.
O ką gi žinome? Atomo sandara ir jos savybės, apie kurias žinome dabar, yra eksperimentų ir stebėjimų derinimo su teorija rezultatas. Kol kas dominuojanti eksperimentinius duomenis paaiškinanti teorija yra standartinis modelis, kuris remiasi kvantinės mechanikos prielaidomis. Čia teigiama, kad atomas yra sudarytas iš elektronų tikimybių debesėlio ir branduolio. Branduolys sudarytas iš protonų ir neutronų. Ir protonai, ir neutronai yra sudaryti iš kvarkų (šiek tiek skirtingų kombinacijų). Kvarkus tarpusavyje laiko stipriąją sąveiką nešančios dalelės – gliuonai, priklausantys bozonų grupei (kitaip tariant, gliuonai neleidžia tą patį krūvį turinčioms dalelėms stumti vienoms kitų).
Taigi atomas yra sudėtinga sistema, kurią „sukišti“ į vieną modelį ne taip ir lengva. Bet klausimas, kodėl mums taip patinka Bohro modelis, išlieka neatsakytas. Kodėl googlindami atomą neiškart pamatome tikimybių debesėlius, bangas arba kvarkų sąveiką? Ką mums duoda Bohro modelis ir ko neduoda kiti?
Simetrija ir Saulės sistema
Dar kartą pažvelkime į Bohro modelį. Matome simetrišką sistemą, sudarytą iš rutulių ir linijų. Vieni rutuliai – stabilūs – susispietę centre, o kiti rutuliai skrieja aplink.
Ir centro stabilumas, ir periferijos judrumas yra ne objektai, o savybės. Visai kitaip esti de Broiglio modelyje: čia judesys (linija, reprezentuojanti bangą) užima materijos vietą. De Broiglio modelis mums pateikia vaizdą, kuris priverčia kvestionuoti vieną iš intuityvių suvokimų apie pasaulį – jog judesys ir objektas yra iš esmės skirtingi. Schrödingerio modelis dar sudėtingesnis – čia judesį pakeičia tikimybės. Su tikimybiniu modeliu statistiniam žiūrovui dar sunkiau susitaikyti negu su sąvoka „banga vietoje materijos“, mat kasdieniame pasaulyje neturime atitikmens tokio buvimo būdo, kurį demonstruoja elementariosios dalelės (t. y. mes esame įpratę, kad daiktai arba yra, arba nėra, o kvantinio pasaulio objektai egzistuoja, bet egzistuoja tik jiems būdingu būdu).
Bohro modelis iš kitų išsiskiria ir savo simetrija, o dalelių išsidėstymas netgi šiek tiek primena „in ir jang“ simbolį. Ir ne vien savo išvaizda! Kinų mąstyme in ir jang – sąveika dviejų lygių, bet priešingų jėgų, kurios sudaro tikrovės pagrindą. Kadangi atome esama dviejų skirtingų krūvių dalelių (elektronų ir protonų), kurių krūvių suma lygi 0, panašumas su in-jang simboliu kuria įspūdį, kad atomas – harmoninga sistema. Vis dėlto tokių sistemų, kaip atomai, siejimas su „tamsos-šviesos“, „vyriškumo-moteriškumo“, „racionalumo-intuicijos“ ir pan. kategorijomis yra neadekvatus ir gali būti netgi ydingas (pavyzdžiui, įsivaizdavimas, kad „tamsioji medžiaga“ yra kažkas bloga).
Į ką dar panašus Bohro modelis? Žinoma, į Saulės sistemą – planetos skrieja aplink Saulę, kaip elektronai aplink branduolį. Žinios apie Saulės sistemą panašios į žinias apie atomą tuo, kad abi šios sistemos pristatomos kaip natūralaus pasaulio reiškiniai, susiję su mumis, tačiau jusliškai tiesiogiai nepatiriami. Mikrosistemų ir makrosistemų (tariamas) panašumas sukuria atpažįstamumo jausmą. Įsitikinimas, kad abi sistemos yra panašios, ne tik sukuria simetrijos, harmonijos įspūdį, bet ir pastato žmogų į Visatos centrą. Tarp dviejų pasikartojančių sistemų (viena sudaro žmogų, kitos dalis yra jis pats) žmogus gali jaustis unikalus, tarsi „globojamas“ reiškinių, kurių tiesiogiai patirti negali.
Taigi kuo mums patinka Bohro modelis? Jis neverčia mūsų kvestionuoti įprastų prielaidų – jei daiktas, tai daiktas, jei banga, tai banga. Jis sukuria harmonijos, priešybių vienybės įspūdį. Jis panašus į Saulės sistemą, taigi sukuria atpažįstamumo, saugumo įspūdį. Be to, Bohro modelis gali būti puiki pradžia, įvadas, norint pažinti atomą. Tačiau norint žinoti daugiau verta turėti omenyje Richard Feynman citatą: „Taigi buvo atrasta, kad mažų objektų elgesys visiškai niekuo nepanašus į didelių objektų elgesį. Štai dėl ko fizika yra tokia sudėtinga – ir tokia įdomi.“
Literatūros sąrašas:
BURNES, Kevin. Rytų filosofija.
FEYNMAN, Richard P. Six easy pieces.
MERIONAS, Dž. B. Fizika ir fizikinis pasaulis. 2.
PIPINYS, Povilas. Kvarkai ir leptonai.





Visai nieko darbelis. Nėra nepakeliamai ilgas, su paveiksliukais ir, o stebukle, atliktas merginos :) Beveik visi sėkmės recepto ingredientai.
patrvitinti -> patvirtinti
Dėkui, klaidelę pataisiau.
Banguojanti meile atomams ;)
Labai patiko!
Šaunus straipsnis! Tokia pat ir parašiusioji :)